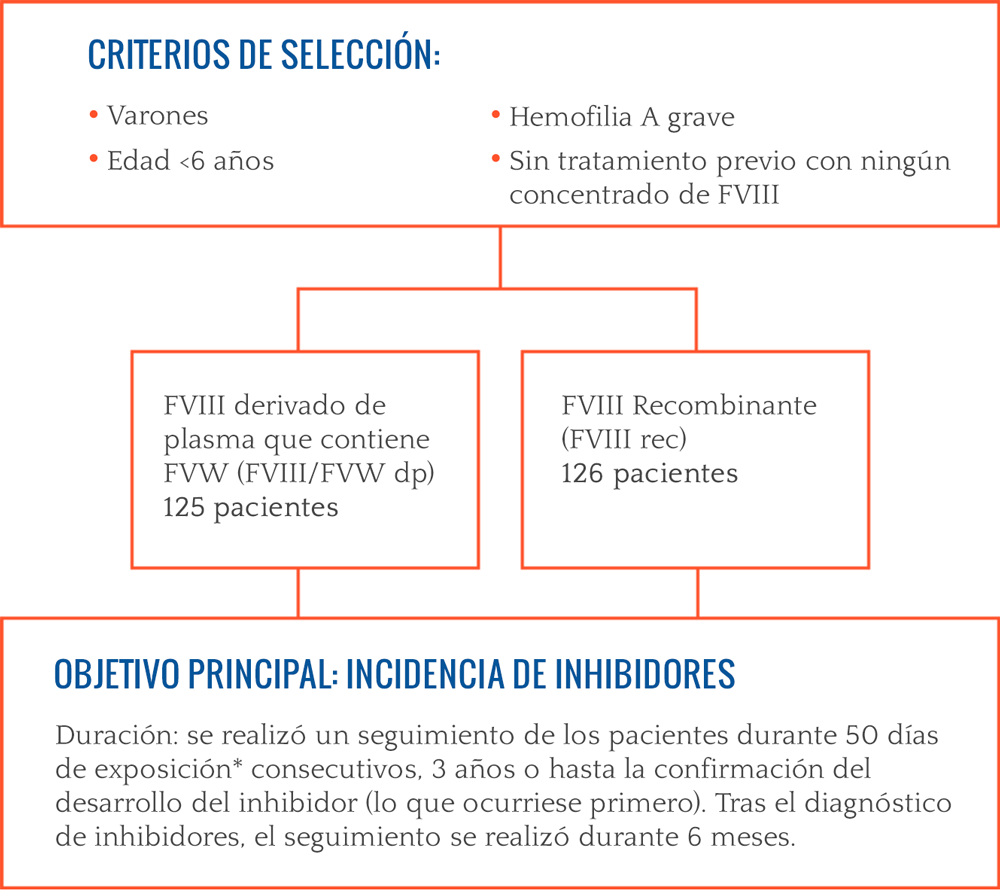
El estudio SIPPET responde una importante pregunta
Los investigadores han dado un gran paso hacia el mayor conocimiento del desarrollo de los inhibidores con los resultados del primer estudio aleatorizado diseñado específicamente para comparar la inmunogenicidad de las diferentes clases de concentrados de FVIII.
El estudio SIPPET, ha demostrado que los pacientes tratados con FVIII plasmático con FVW experimentaron una incidencia significativamente menor de inhibidores que los tratados con FVIII recombinante.1
Estos resultados son importantes clínicamente, ya que el desarrollo de inhibidores es la principal complicación en el tratamiento de la hemofilia A.1
EL CAMINO HASTA EL ESTUDIO SIPPET: UNA PERSPECTIVA HISTÓRICA
Con los años, la investigación clínica ha tratado de responder una pregunta importante: ¿afecta a la probabilidad de desarrollar inhibidores el origen del producto de FVIII usado en el tratamiento? Los estudios publicados hasta la fecha han mostrado disparidad en los datos cuando se comparaba la inmunogenicidad de los distintos tipos de FVIII, derivados del plasma y recombinantes.1-4
Los investigadores Wight y Paisley revisaron la evidencia publicada hasta 2003. El análisis de 50 estudios en pacientes no tratados previamente, corroboró la clara evidencia de que los diferentes productos de FVIII tenían distinta inmunogenicidad, siendo los productos derivados del plasma menos inmunogénicos que los productos recombinantes.
En 2006 se publicó el estudio CANAL, un estudio retrospectivo observacional que incluyó 316 pacientes con hemofilia A grave no tratados previamente. CANAL concluyó que el riesgo de desarrollar inhibidores era ligeramente inferior con productos derivados del plasma en comparación con los productos recombinantes. Aunque la diferencia no fue estadísticamente significativa.
Posteriormente, en 2013 se publicó el estudio RODIN, un estudio observacional prospectivo que incluyó 574 pacientes nacidos entre 2000 y 2010 no tratados previamente. Los resultados no mostraron diferencias en el riesgo de desarrollar inhibidores con FVIII derivado del plasma frente al FVIII recombinante. Sin embargo, RODIN no fue un ensayo clínico aleatorizado y tan solo el 15 % de los pacientes incluidos recibió tratamiento con un FVIII derivado del plasma.
LA PREGUNTA CONTINUABA SIN RESPUESTA
Algunos ensayos demostraban que los productos de FVIII derivados del plasma que contienen FVW pueden reducir el riesgo de desarrollar inhibidores, pero los estudios observacionales que precedieron a SIPPET no pudieron confirmarlo. Sin embargo, estos estudios no estaban controlados, lo que significa que posiblemente otros factores de riesgo y causas sesgaban los resultados, haciéndolos no concluyentes. Fue necesario el dato concluyente del estudio SIPPET para demostrar si había una diferencia en el desarrollo de inhibidores entre el FVIII recombinante y el FVIII derivado del plasma en pacientes sin tratamiento previo. 1
RESULTADOS DEL ESTUDIO SIPPET1
El estudio SIPPET, ha demostrado que los pacientes tratados con FVIII plasmático con FVW tienen una incidencia significativamente menor de inhibidores que los tratados con FVIII recombinante. La tasa de desarrollo de inhibidores con el FVIII recombinante fue casi del doble que con el FVIII derivado del plasma con FVW.
Los autores concluyeron que estos resultados pueden tener implicaciones en el tratamiento de los pacientes previamente no tratados.
Incidencia de inhibidores
FVIII/FVW dp
125 pacientes
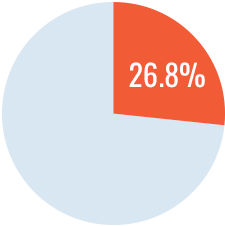
FVIII rec
126 pacientes
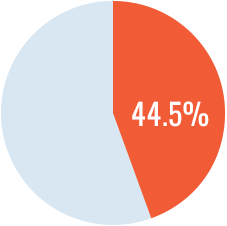
 Pacientes con inhibidores
Pacientes con inhibidores
Incidencia de inhibidores 87 % más alta con FVIII recombinante comparado con FVIII derivado del plasma con FVW.
(HR = 1,87 IC95: 1,17-2,96)1
IMPLICACIONES CLÍNICAS
El FVIII/FVW derivado del plasma humano y por tanto de origen natural, demostró un desarrollo de inhibidores significativamente menor que el FVIII recombinante diseñado en líneas celulares de origen animal, en pacientes previamente no tratados. Este resultado es clínicamente relevante, ya que el desarrollo de inhibidores es la complicación más grave hoy en día en el tratamiento de la hemofilia A.1
La elección del producto es importante en relación con el riesgo de desarrollar inhibidores1
Los resultados de SIPPET pueden cambiar la forma en la que los profesionales sanitarios planteen los tratamientos, especialmente en pacientes sin tratamiento previo.
Los productos derivados del plasma que contienen FVW pueden ser inmunoprotectores1
Los resultados de SIPPET reflejan los hallazgos de algunos ensayos que demuestran que la presencia del FVW en productos derivados del plasma puede proteger al paciente frente al desarrollo de inhibidores.
Recomendaciones de las sociedades científicas
Las actuales recomendaciones de tratamiento de la hemofilia y el uso de FVIII derivado del plasma frente al FVIII recombinante, pueden ser modificadas para reflejar estos nuevos hallazgos en el desarrollo de inhibidores. Inscríbase en InhibitorInfo.com para recibir las recomendaciones actualizadas.
IMPLICACIONES CLÍNICAS
El FVIII/FVW derivado del plasma humano y por tanto de origen natural, demostró un desarrollo de inhibidores significativamente menor que el FVIII recombinante diseñado en líneas celulares de origen animal, en pacientes previamente no tratados. Este resultado es clínicamente relevante, ya que el desarrollo de inhibidores es la complicación más grave hoy en día en el tratamiento de la hemofilia A 1
La elección del producto es importante en relación con el riesgo de desarrollar inhibidores1
Los resultados de SIPPET pueden cambiar la forma en la que los profesionales sanitarios planteen los tratamientos, especialmente en pacientes sin tratamiento previo.
Los productos derivados del plasma que contienen FVW pueden ser inmunoprotectores1
Los resultados de SIPPET reflejan los hallazgos de algunos ensayos que demuestran que la presencia del FVW en productos derivados del plasma puede proteger al paciente frente al desarrollo de inhibidores.
Recomendaciones de las sociedades científicas
Las actuales recomendaciones de tratamiento de la hemofilia y el uso de FVIII derivado del plasma frente al FVIII recombinante, pueden ser modificadas para reflejar estos nuevos hallazgos en el desarrollo de inhibidores.
BIBLIOGRAFÍA
- Peyvandi F, Mannucci PM, Garagiola I, et al. A randomized trial of factor VIII and neutralizing antibodies in hemophilia A. N Engl J Med. 2016;374(21):2054-2064.
- Wight J, Paisley S. The epidemiology of inhibitors in haemophilia A: a systematic review. Haemophilia. 2003;9:418-435.
- Gouw SC, van der Bom JG, Auerswald G, Ettinghausen CE, Tedgård U, van den Berg HM for the CANAL Study Group. Recombinant versus plasma-derived factor VIII products and the development of inhibitors in previously untreated patients with severe hemophilia A: the CANAL cohort study. Blood. 2007;109(11):4648-4654.
- Gouw SC, van der Bom JG, Ljung R, et al, for; the PedNet and RODIN Study Group. Factor VIII products and inhibitor development in severe hemophilia A. New Engl J Med. 2013;368(3):231-239.