Estudios clínicos en ITI
Estudios con concentrados de FVIII con FVW de origen plasmático

"Immune tolerance induction with a high purity von Willebrand factor/VIII complex concentrate in haemophilia A patients with inhibitors at high risk of a poor response."1
Gringeri A. Haemophilia 2007
- Objetivo: identificar la efectividad de un concentrado de alta pureza de FVIII con FVW de origen plasmático en ITI en pacientes con inhibidores y alto riesgo de fracaso.
-
Diseño: estudio multicéntrico, observacional y prospectivo.
- Pacientes incluidos en el estudio: 16 con hemofilia A grave; 1 con hemofilia A moderada.
- Edades de entre 4-54 años.
- Seguimiento de los pacientes desde 6 - 71 meses.
-
Resultados:
- La tasa de éxito* total fue del 94 % (tasa éxito completo + tasa éxito parcial)
- 53 % de éxito completo en ITI y 41 % de éxito parcial en ITI
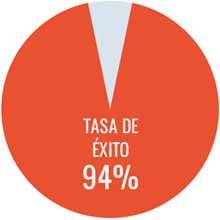
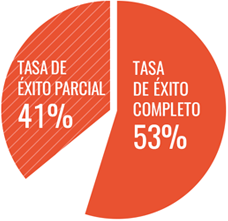
*Tasa de éxito completo: titulo <0.5 BU en al menos 2 mediciones consecutivas mensuales con confirmación en laboratorio central, y recuperación y vida media >66%.
Tasa de éxito parcial: Pico de inhibidor no mayor de 3 BU y recuperación y vida media <66%.
Fracaso: Reducción de titulo BU <20% en los 9 meses siguientes al pico de respuesta amnésica.

"The use of a single von Willebrand factor-containing, plasma-derived FVIII product in hemophilia A immune tolerance induction: the US experience."2
Kurth M. Thromb Haemost. 2011
- Objetivo: reportar datos retrospectivos sobre el uso de un único concentrado plasmático de FVIII con FVW en ITI primaria y secundaria o de rescate.
- Diseño: estudio independiente, multicéntrico, observacional y retrospectivo.
-
Resultados:
-
Tasas de éxito*
- - ITI primaria: 8 pacientes con un éxito (completo o parcial)* del 75 %.
- - ITI secundaria: 25 pacientes con un éxito (completo o parcial)* del 52 %.
-
Tasas de éxito*
Tasa de éxito de la ITI primaria
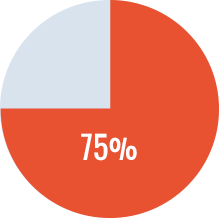
*Tasa de éxito completo: titulo <0.6 BU, recuperación ≥66%, y vida media >6 hr
Tasa de éxito parcial: titulo <5 BU
Fracaso: Reducción de titulo BU <20% en los 6 meses siguientes al tratamiento tras 3 meses de inicio del tratamiento.

"Primary and rescue ITI in children and adults: a multicenter international study with a VWF-containing plasma-derived FVIII concentrate."3
Oldenburg J. Haemophilia 2014
- Objetivo: reportar los resultados retrospectivos en adultos y niños sobre el uso de un único concentrado plasmático de FVIII con FVW en ITI primaria y de rescate.
-
Diseño: estudio internacional, multicéntrico, observacional y retrospectivo.
- Pacientes incluidos en el estudio 60 con hemofilia A (FVIII <2 %).
- ITI primaria en 41 pacientes: 32 niños y 9 adultos.
- ITI de rescate en 19 pacientes: 17 niños y 2 adultos.
-
Resultados:
-
Tasa de éxito total* del 84 % (tasa éxito completo + tasa éxito parcial)
- - Tasa de éxito en ITI primaria 87%
- - Tasa de éxito en ITI de rescate 67%
-
Tasa de éxito total* del 84 % (tasa éxito completo + tasa éxito parcial)
Tasa de éxito
total
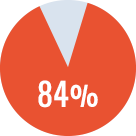
Tasa de éxito de la
ITI primaria
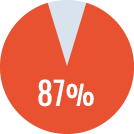
Tasa de éxito de la
ITI secundaria
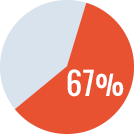
*Tasa de éxito completo: título <0.6 BU a los 33 meses, recuperación ≥66% y vida media >6 hr.
Tasa de éxito parcial: titulo <5 BU, recuperación < 66% y vida media <6 hr asociada a respuesta clínica al FVIII
Fracaso: No consecución de los anteriores .

"Adult hemophilia A patients with inhibitors: successful ITI with a single FVIII/VWF product"4
Rangarajan S. Haemophilia 2014
- Objetivo: evaluar retrospectivamente el éxito de ITI (primaria y de rescate) en una cohorte de adultos.
- Diseño: estudio observacional y retrospectivo en 20 pacientes adultos.
-
Resultados:
-
Tasas de éxito* total del 90 %
- ITI primaria en 17 pacientes: tasa de éxito del 94 %
- ITI de rescate en 3 pacientes: tasa de éxito del 66 %
-
Tasas de éxito* total del 90 %
Tasa de éxito
total

Tasa de éxito de la
ITI primaria
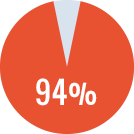
Tasa de éxito de la
ITI secundaria
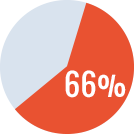
*Tasa de éxito completo: título no detectable <0.6 BU a los 33 meses, recuperación ≥66% y vida media >6 h.
Tasa de éxito parcial: titulo <5 BU, recuperación < 66% y vida media <6 hr asociada a respuesta clínica al FVIII
Fracaso: No consecución de los anteriores .

"First prospective report on immune tolerance in poor risk haemophilia A inhibitor patients with a single factor VIII/von Willebrand factor concentrate in an observational immune tolerance induction study"5
Kreuz W. Haemophilia 2016
- Objetivo: evaluar prospectivamente el éxito de ITI, como tratamiento estándar en pacientes con inhibidores y factores de riesgo.
-
Diseño: Observacional, prospectivo, no controlado, abierto, internacional.
- Pacientes incluidos en el estudio: 48
-
Resultados:
- Tasa de éxito total del estudio: 77%
- 40 de los 48 pacientes (83,3 %) tenían al menos un factor de riesgo de mal pronóstico al inicio de la ITI.
- 34 pacientes (70.8%) alcanzaron la tasa de éxito completa*, 3 (6.3%) alcanzaron un éxito parcial**, 1 (2.1%) alcanzo una respuesta parcial ***, La ITI no funcionó en 10 pacientes (20,8 %), todos ellos con factores de mal pronóstico.
- Todos los pacientes que tenían inhibidores de baja respuesta lograron un éxito completo.
Tasa de éxito total
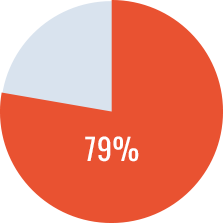
*Tasa de éxito completo: Requiere alcanzar los 3 criterios de eficacia
**Tasa de éxito parcial: Requiere al menos 2 de los 3 criterios
***Respuesta parcial: Requiere al menos 1 de los 3 criterios
Fracaso: No se cumple ningún criterio en los 36 meses de periodo observacional.
Criterios de eficacia:
- Criterio 1: titulo <0.6 BU
- Criterio 2: recuperación ≥80% en los valores de referencia predefinidos de 1.5% IU /kg tras ≤1 h de infusión
- Criterio 3: vida media ≥7 h

"Long-Term Outcome of Haemophilia A Patients After Successful Immune Tolerance Induction Therapy using a Single Plasma-Derived FVIII/VWF Product: The Long-Term ITI Study"6
Jimenez-Yuste V. Haemophilia 2016
- Objetivo: Analizar retrospectivamente y a largo plazo el estado de los pacientes que lograron con éxito la inmunotolerancia en el estudio G- ITI3 (Oldenburg Haemophilia 2013)
-
Diseño: Internacional, multicéntrico, observacional, retrospectivo.
- Pacientes incluidos en el estudio: 44
-
Resultados:
- La media del periodo de seguimiento tras el éxito* de la ITI fue 9,3 ± 3,3 años (2,1-17,7).
- El tratamiento preferente tras la consecución de la ITI fue la profilaxis en más del 93% de los pacientes.
- Tan solo 3 de 44 pacientes (6.8%) presentaron recidiva en la aparición de inhibidores.
Recidiva de inhibidores
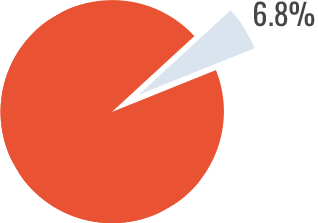
Estudios con concentrados de FVIII de origen recombinante

"Immune tolerance induction with recombinant factor VIII in hemophilia A patients with high responding inhibitors."7
Rocino A. Haematologica 2006
-
Objetivo:
- Evaluar la tasa de éxito de la ITI con concentrados de FVIII recombinantes en pacientes con hemofilia A grave e inhibidores con buena respuesta.
- Obtener datos sobre la posible relación entre las mutaciones del gen F8 y el resultado de la ITI así como de otros factores que pueden influir en el resultado.
-
Diseño: estudio multicéntrico y observacional en 26 pacientes que se sometieron a ITI.
- Las pautas de ITI oscilaron entre 50 UI/kg de FVIII cada dos días hasta 200 UI/kg al día, con 17 pacientes (65 %) que recibían 100 UI/kg al día.
-
Resultados:
- Tasa de éxito* :73%
- 70 % para los pacientes con inversión del intrón 22
Tasa de éxito total
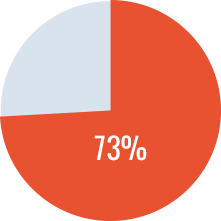
*Tasa de éxito si se cumplen los criterios: no detección de actividad inhibitoria, normalización de la recuperación in vivo >66% y vida media > 6 h
Tasa de éxito parcial: no detección de actividad inhibitoria pero sin normalización de la recuperación in vivo < 66% y vida media < 6 h
Fracaso: presencia de inhibidor durante 6 meses tras los primeros 3 meses de tratamiento

"Experience with a third generation recombinant factor VIII concentrate for immune tolerance induction in patients with haemophilia A."8
Valentino LA. Haemophilia 2009
- Objetivo: evaluar retrospectivamente la tasa de éxito de ITI con un concentrado de FVIII recombinante de tercera generación en niños con hemofilia A grave.
- Diseño: Estudio retrospectivo. Pacientes incluidos en el estudio: 12 niños con hemofilia A grave, que desarrollaron inhibidores y fueron tratados durante un período de 30 meses.
-
Resultados:
- Tasa de éxito* : 7 %
- Se obtuvo una tasa de éxito del 70 % en los pacientes con títulos altos de inhibidores y del 100% en aquellos con título bajo.
Tasa de éxito total

* Tasa de éxito: no detección de actividad inhibitoria (<0.6 BU mL), recuperación ≥66% en plasma y vida media ≥6 h tras 72h de periodo de lavado y en ausencia de anamnesis tras exposición a FVIII.

"Principal results of the International Immune Tolerance Study: a randomized dose comparison"9
Hay CR. Blood 2012
- Objetivo: Verificar la hipótesis de que la respuesta a la ITI es independiente de la pauta posológica de FVIII en pacientes con pronóstico favorable.
-
Diseño: estudio multicéntrico, prospectivo y aleatorizado para comparar dosis altas (DA) y dosis bajas (DB) de tratamiento.
- Pacientes incluidos en el estudio: 115
- Todos los pacientes tenían ≤8 años, hemofilia A grave y títulos altos de inhibidores
- Se utilizó FVIII recombinante en el 90 % de los casos y FVIII con FVW plasmático en tan solo el 10 %.
-
Resultados:
- Las tasa de éxito* fue del 74% y no difirió entre los distintos grupos de tratamiento.
- La DB aumentó las complicaciones de hemorragia en comparación con la DA. El ratio de sangrados mensual fue de 0.62 (DB) frente a 0.28 (DA), decreciendo hasta en un 90% cuando se alcanzaron los títulos negativos
- Con DA se alcanzó más rápido la erradicación del inhibidor y la recuperación de FVIII que con DB. El tiempo medio para alcanzar la tasa de éxito fue menor en los pacientes en DA (14.2 meses) que en aquellos en régimen de DB (16.4 meses).
Tasa de éxito total
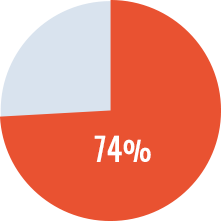
* Tasa de éxito: título BU negativo, recuperación ≥66% y vida media ≥6 h tras
Tasa de éxito parcial: tras 33 meses de tratamiento título BU negativo con recuperación o vida medias deficientes pero con respuesta clínica a FVIII y sin anamnesis o incremento del título del inhibidor.
Fracaso: descenso de BU de menos del 20% tras un periodo de 6 meses posteriores a los primeros 3 meses de tratamiento, o imposibilidad de alcanzar la tasa completa o parcial de éxito en 33 meses o retirada del tratamiento por cualquier razón.
Es importante tener en cuenta que el tratamiento varía según el paciente. Asegúrese de consultar a un profesional sanitario antes de tomar cualquier decisión respecto al tratamiento y continúe manteniéndose informado para facilitar su atención médica.
BIBLIOGRAFÍA
- Gringeri A.et al. Immune tolerance induction with a high purity von Willebrand factor/VIII complex concentrate in haemophilia A patients with inhibitors at high risk of a poor response. Haemophilia 2007 Jul; 13(4):373-9.
- Kurth M. et al. The use of a single von Willebrand factor-containing, plasma-derived FVIII product in hemophilia A immune tolerance induction: the US experience. J. Thromb Haemost. 2011 Nov; 9(11):2229-34.
- Oldenburg J. et al. Primary and rescue ITI in children and adults: a multicenter international study with a VWF-containing plasma-derived FVIII concentrate. Haemophilia 2014 Jan; 20(1):83-91.
- Rangarajan S. et al. Adult haemophilia A patients with inhibitors: successful immune tolerance induction with a single FVIII/VWF product. Haemophilia 2014, 20, e399-e443.
- Kreuz W.et al. First prospective report on immune tolerance in poor risk haemophilia A inhibitor patients with a single factor VIII/von Willebrand factor concentrate in an observational immune tolerance induction study. Haemophilia 2016 Jan;22(1):87-95.
- Jimenez-Yuste V. et al. Long-Term Outcome of Haemophilia A Patients After Successful Immune Tolerance Induction Therapy using a Single Plasma-Derived FVIII/VWF Product: The Long-Term ITI Study. Haemophilia 2016. DOI: 10.1111/hae.12986
- Rocino A. et al. Immune tolerance induction with recombinant factor VIII in hemophilia A patients with high responding inhibitors. Haematologica 2006 Apr;91(4):558-61
- Valentino LA. et al. Experience with a third generation recombinant factor VIII concentrate for immune tolerance induction in patients with haemophilia A. Haemophilia 2009 May; 15(3):718-26.
- Hay CR. et al. The principal results of the International Immune Tolerance Study: a randomized dose comparison. Blood 2012 Feb 9; 119(6):1335-44.
